'원료의약품'검색결과 - 전체기사 중 4건의 기사가 검색되었습니다.
-

식약처, ‘2023년 의약품·의료기기 허가 분야 민관 소통 계획’ 발표
식품의약품안전처(처장 오유경)는 의약품·의료기기 업계 현장의 목소리를 듣고 애로사항을 해소하고, 관련 제도개선에도 적극 활용하기 위한 ‘2023년 의약품·의료기기 허가 분야 민·관 소통 계획’을 발표했다. 식약처는 관련 7개 협회*와 함께 의약품·의료기기 허가 분야에서 민·관 소통의 장을 운영하고 있으며, 전문성 확보를 위해 의약품 분야(‘팜투게더’, 2018년부터)와 의료기기 분야(‘소유’, 2019년부터)로 나눠 운영하고 있다. * 한국제약바이오협회, 한국글로벌의약산업협회, 한국의약품수출입협회...
- 이서현
- 2023-02-15 01:36
-

한국 ‘EU 화이트리스트’ 등재 유지, 원료의약품 EU 수출 확대 기대
식품의약품안전처(처장 오유경)는 우리나라가 2019년 세계 7번째로 ‘EU 화이트리스트(GMP* 서면확인서** 면제 국가)’에 등재된 이후 첫 정기 재평가(’22.12.5~9.)에서 등재국 지위를 유지했다. * GMP(제조·품질관리기준): 의약품이 허가받은 사항과 마련된 품질 기준에 따라 일관되게 제조·관리되고 있음을 보증하는 제도 ** GMP 서면확인서: 유럽연합(EU) 비회원국이 EU로 원료의약품을 수출하는 경우 해당 국가 규제당국(예: 식약처(한국))이 제조원에 대해 EU와 동등한 수준(GMP...
- 이서현
- 2023-01-30 23:47
-

식약처, 모든 의약품 대상으로 해외제조소 등록 의무화
식품의약품안전처(오유경 처장)는 의약품의 품질관리 강화를 위해 해외에서 국내로 수입하려는 모든 의약품(원료의약품 포함)의 해외제조소*를 사전에 등록하는 제도를 1월 21일부터 본격 시행**한다. * (해외제조소) 수입 의약품 등에 대한 제조·품질관리를 실시하는 해외에 소재하는 시설 ** 「약사법」 개정(’22.7.20.) → 시행(’22.7.21.) → 시행 유예기간(~’23.1.20) 이는 업계의 준비 상황 등을 고려해 해외제조소 등록 대상을 자사 완제의약품 제조용으로 수입한 원료의...
- 이서현
- 2023-01-21 00:02
-
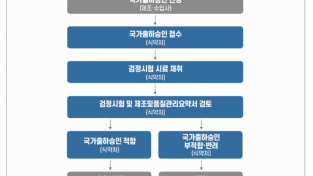
국내 제조 모더나 코로나19 2가 백신 157만 회분 국가출하승인
▲국가출하승인 절차 / 사진 제공: 식약처 식품의약품안전처(처장 오유경)는 모더나코리아사(社)의 국내 제조 mRNA 코로나19 2가 백신인 ‘스파이크박스2주(엘라소메란, 이멜라소메란)’ 157만 회분에 대해 10월 11일 국가출하승인했다고 밝혔다. 국가출하승인이란 백신이 시중에 유통되기 전에 제조단위(로트)별로 국가가 검정시험한 결과 제조사의 제조·시험 결과를 종합적으로 평가해 품질을 한 번 더 확인하는 제도이다. 참고로 ‘스파이크박스2주’는 지난 9월 8일 수입 허가받은 ‘모더나스파이크박스2주’와 같은 원료의약...
- 김승현
- 2022-10-12 21:53

![[특집-ISO/IEC JTC 1/SC 17 활동] 35. Result of voting on SR Ballot for ISO/IEC 7811-7(N 7345) [특집-ISO/IEC JTC 1/SC 17 활동] 35. Result of voting on SR Ballot for ISO/IEC 7811-7(N 7345)](http://www.stdnews.kr/data/file/news/thumb-3555379571_4cufp2BH_756bcefa64e6169e58646ad7b061ecbec455fb11_118x78.jpg)

![[잘난척아는척TV] 충전기 타입이 자꾸 바뀌는 이유 [잘난척아는척TV] 충전기 타입이 자꾸 바뀌는 이유](http://www.stdnews.kr/data/file/news/thumb-661839498_b09ltrRW_d5e36bb7755deae8f2d0fd06db3041a3e97ed9f8_118x78.jpg)
![[특집-기상기후재난] 한국중부발전(주) 신정철 선임 인터뷰 - 행정안전부 뿐 아니라 기상기후 연계조직 모두가 참여하는 협의체가 돼야 [특집-기상기후재난] 한국중부발전(주) 신정철 선임 인터뷰 - 행정안전부 뿐 아니라 기상기후 연계조직 모두가 참여하는 협의체가 돼야](http://www.stdnews.kr/data/file/news/thumb-3555374516_iKWwUBas_9c1729f1e3977ee50c398986e7f98d5002a57deb_118x78.jpg)

![[잘난척아는척TV] 평생 아무도 알려주지 않은 첫째 주 목요일은 언제일까? [잘난척아는척TV] 평생 아무도 알려주지 않은 첫째 주 목요일은 언제일까?](http://www.stdnews.kr/data/file/news/thumb-2948726586_UkXaF364_18ad3c8e673eb23da0e5df66ebf7fd2a8317fdb4_190x190.jpg)

